Modifikasi Pada Gugus Amina Dan Imina
AMINA
Amina adalah turunan organik dari ammonia dimana satu atau lebih atom hidrogen pada nitrogen telah tergantikan oleh gugus alkil atau aril. Karena itu amina memiliki sifat mirip dengan ammonia seperti alkohol dan eter terhadap air. Seperti alkohol,amina bisa diklasifikasikan sebagai primer, sekunder dan tersier. Meski demikian dasar dari pengkategoriannya berbeda dari alkohol. Alkohol diklasifikasikan dengan jumlah gugus non hidrogen yang terikat pada karbon yang mengandung hidroksil., namun amina diklasifikasikan dengan jumlah gugus nonhidrogen yang terikat langsung pada atom nitrogen (Stoker, 1991).
Dengan demikian kelompok fungsional karakteristik untuk amina primer, sekunder dan tersier adalah:
CH3CH2NH2 + CH3CO2H CH3CH2NH3 -O2CCH3
etilamonium asetat atau etilamina aseta
34.5OC 56OC 117OC
Karena itu mempunyai ikatan NH, amina tersier dalam bentuk cairan murni tidak dapat membentuk ikatan hidrogen. Titik didih amina tersier lebih rendah dari pada amina primer atau sekunder yang bobot melekulnya sepadan, dan titik didihnya lebih dekat ke titik didih alkana yang bobot molekulnya bersamaan. Dan amina yang berbobot molekul rendah larut dalam air karena membentuk ikatan hidrogen dengan air. Amina tersier maupun amina sekunder dan primer dapat membentuk ikatan hidrogen karena memiliki pasangan elektron menyendiri yang dapat digunakan untuk membentukikatan hidrogen dengan air.
Dan berikut merupakan beberapa sifat fisis amina
Nama
|
Struktur
|
Titik Didih oC
|
Kelarutan dalam air
|
Metilamina
|
CH3NH2
|
-6.3
|
∞
|
Dimetilamina
|
(CH3)2NH
|
7.5
|
∞
|
Trimetilamina
|
(CH3)3N
|
3
|
∞
|
Etilamina
|
CH3CH2NH2
|
17
|
∞
|
Benzilamina
|
C6H5CH2NH2
|
185
|
∞
|
Anilina
|
C6H5NH2
|
184
|
37 /100 ml
|
PEMBUATAN AMINA
à Cara Reaksi Reduksi
a. Pembuatan amina primer
Untuk pembuatan amina primer, reaksi terjadi dalam dua tahapan. Pada tahapan pertama, terbentuk sebuah garam – dalam hal ini, etilamonuim bromida. Garam ini sangat mirip dengan amonium bromida, kecuali bahwa salah satu atom hidrogen dalam ion amonium telah diganti oleh sebuah gugus etil. Dengan demikian, ada kemungkinan untuk terjadinya reaksi reversibel (dapat balik) antara garam ini dengan amonia berlebih dalam campuran. Amonia mengambil sebuah atom hidrogen dari ion etilamonium sehingga menjadikannya amina primer, yakni etilamina. Semakin banyak amonia yang terdapat dalam campuran, semakin besar kemungkinan terjadi reaksi selanjutnya.
b. Pembuatan amina sekunder
Reaksi di atas tidak berhenti setelah amina primer terbentuk. Etilamina juga bereaksi dengan bromoetana – dalam dua tahapan yang sama seperti reaksi sebelumnya. Pada tahap pertama, terbentuk sebuah garam – kali ini, dietilamonium bromida. Anggap garam yang terbentuk ini adalah amonium bromida dengan dua atom hidrogen yang digantikan oleh gugus-gugus etil.
Lagi-lagi terdapat kemungkinan terjadinya reaksi reversibel (dapat balik) antara garam ini dengan amonia berlebih dalam campuran tersebut, seperti diperlihatkan pada gambar berikut: Amonia mengambil sebuah ion hidrogen dari ion dietilamonium sehingga menjadikannya amina sekunder, yakni dietilamin. Amina sekunder adalah amina yang memiliki dua gugus alkil terikat pada atom nitrogen.
a. Pembuatan amina tersier
Setelah amina sekunder terbentuk, reaksi masih belum berhenti. Dietilamina juga bereaksi dengan bromoetana – dalam dua tahapan yang sama seperti pada reaksi sebelumnya.Pada tahapan pertama, terbentuk trietilamonium bromida.Lagi-lagi ada kemungkinan terjadinya reaksi reversibel (dapat balik) antara garam ini dengan amonia berlebih dalam campuran tersebut, sebagaimana ditunjukkan berikut: Amonia mengambil sebuah ion hidrogen dari ion trietilamonium sehingga menjadikannya amina tersier, yakni trietilamin. Amina tersier adalah amina yang memiliki tiga gugus alkil terikat pada nitrogen.
Reaksi Substitusi Dengan Amina
Ikatan dalam amina
Ikatan dalam suatu amina beranalogi langsung dengan ikatan dalam amonia, suatu atomnitrogen sp3 yang terikat pada tiga atom atau gugus lain (H atau R) dan dengan sepasang elektronmenyendiri dalam orbital sp3 yang tersisa.
Dalam garam amina atau garam amonium kuartener,pasangan elektron menyendiri memembentuk ikatan sigma keempat. Kation beranalogi dengan ion amonium.
Suatu molekul amina dengan tiga gugus berlainan yang terikat pada nitrogen akan bersifat kiral;namin,enantiomer dari sebagian besar senyawa amina tidak dapat diisolasi karena terjadinya inverse yang cepat antara bayangan-bayangan cermin pada temperatur kamar. Inversi itu berlangsung lewat keadaan-transisi datar (nitrogen sp2). Akibatnya ialah piramida nitrogen itu menjentik sehingga dindingdalam menjadi dinding luar, mirip payung yang terhenbus angin kencang. Energi yang diperlukan untuk inversi ini sekitar 6 kkal/mol, kira-kira dua kali energi untuk rotasi mengelilingi ikatan sigma karbon-karbon.
Jika suatu nitrogen amina mempunyai tiga substituen yang berlainan dan pengubahan timbalbalik antara kedua struktur bayangan cermin itu terhalang, maka dapatlah diisolasi sepasang enantiomer. Basa Troger adalah suatu contoh molekul semacam itu. Titian metilena antara kedua nitrogen mencegah pengubahan timbalbalik (inverkonversi) antara banyangan cermin, sehingga basa Troger dapat dipisahkan menjadi sepasang enantiomer.
Kasus lain dimungkinkan adanya enantiomer yang dapat diisolasi ialah pada garam amonium kuterner. Senywa ini secara struktur mirip senywa yang mengandung atom karbon sp3. Jika empat gugus yang berlainan terikat pada nitrogen, ion itu akan bersifat kiral dan garam itu dapat dipisah sebagai enantiomer – enantiomer.
Penggunaan amina dalam sintesis
Sintesis senyawa yang mengandung nitrogen mendapatkan perhatian khusus dari para ahli kimia organik yang berkecimpung dalam farmakologi dan ilmu pngetahuan biologis lainnya, karena banyak biomolekul yang mengandung nirogen. Sebagian besar yang digunakan untuk mensintesis senyawa nitrogen dari amina telah dibahas dalam buku lain.
Banyak reaksi amina adalah hasil serangan nukleofilik oleh elektron menyendiri dari nitrogen amina. Reaksi substitusi suatu amina dengan alkil halida adalah suatu contoh dari amina yang bertindak sebagai suatu nukleofil. Amina dapat juga digunakan sebagai nukleofil dalam reaksi substitusi asil nukleofilik. Jika derivat asam karboksilat merupakan reagensia karbonilnya, maka diperolehamida sebagai produk. Jika reaksi karbonil berupa aldehid atau keton, produknya dalah imina (dari amina primer, RNH2) atau suatu enamina (dari suatu amina sekunder, R2NH).
-NR3+OH-) merupakan suatu teknik sintetik lain. Eliminasi Hofmann dari amonium kuarter hidroksida, lebih berguna sebagai suatu alat analitis dari pada suatu alat sintetik, karena dihasilkan campuran alkena. (juga, suatu reaksi eliminasi alkil halida merupakan jalur yang lebih mudah menuju alkena di laboratorium). Bahkan spektroskopi nmr telah lebih bayak digunakan sebgai suatu alat bantu dalam suatu struktur dari pada eliminasi Hofmann. Di pihak lain,pengubahan suatu arilamina menjadi garam diazonium yang disusul reaksi substitusi, sangat berguna dalam sitesis organik, dan untuk memeriksa tipe senyawa yang mudah diperoleh dari garam arildiazonium.
Enantiomer tunggal dari amina kristal lazim dijumpai dalam tumbuhan. Karena kebasaannya, beberapa amina ini dapat digunakan untuk memisahkan asm-asam karboksilat rasimik. Dua diantaranya ialah striknina (strychnine) dan brusina (brucine), keduanya dapat diisolasi dari biji bidara laut (strychnos nux-vomica; kedua senyawa itu merupakanstimulan yang bersifat racun dalam sistem syaraf pusat). Berikut adalah beberapa senyawa yang dapat diperoleh dari amina:
- Garam amina
- Amida
- Imida
- Enamina
- Garam arildiazonium
- Alkena
R3N + R’X R3NR’X- (Garam Amina)
| ||
O O
R2NH + R’CCl R2NCR’ (Amida)
| ||
RNH2 primer + R’2C O RN CR’2 (Imina)
| ||
O NR2
R2NH sekunder + R’2CHCR’ R’2C CR’ (Enamina)
| ||
ArNH2 ArN2+Cl- (Garam Arildiazonium)
| ||
NR’2
R2CHCR2 R2C CR2 (Alkena)
|
GARAM AMINA
Garam yang terbentuk oleh amina adalah zat kristal yang dapat segera larut dalam air. Larut Banyak alkaloid (misalnya kina dan atropin) digunakan medicinally dalam bentuk garam larut ('hydrochlorides'). Jika alkali (natrium hidroksida) ditambahkan ke larutan garam seperti amina bebas adalah dibebaskan.
Reaksi suatu asam amina dengan suatu asam mineral (seperti CHl) atau suatu asam karboksilat (seperti asam asetat) menghasilkan suatu garam amina. Garam amina lazim diberi nama menurut salah satu dari dua cara: sebagai garam ammonium tersubstitusi atau sebagai kompleks amina-asam.
(CH3)3N: + HCl (CH3)3NH+ Cl-
trimetilamonium klorida atau trimetilamina hidroklorida
CH3CH2NH2 + CH3CO2H CH3CH2NH3 -O2CCH
etilamonium asetat atau etilamina aseta
Amonia termasuk nukleofil yang dapat menyerang karbon maupun gugus karbonil yang berasal dari aldehid maupun keton. Pada reaksinya dikatalis oleh runutan asam, sehingga tahap pertama dalam reaksi itu dapat disebut sebagai adisi sederhana oleh ammonia terhadap gugus karbonil tersebut. Sehingga hasil adisi yang tidak stabil akan melepaskan air dan menghasilkan suatu imina, yaitu suatu senyawa yang mengandung gugus C=N. Senyawa amina primer yang bereaksi dengan aldehid dan keton akan menghasilkan suatu senyawa imina. Pembentukan suatu imina secara mekanisme mirip dengan reaksi aldol. Pembentukan imina dikatalis oleh asam encer. Reaksinya dapat berjalan secara optimal pada pH 3-5.
Mengapa reaksi berjalan optimum pada pH dengan keasaman tinggi, karena amina merupakan nukleofilik sehingga terdapat sepasang electron bebas yang terdapat pada atom nitrogen. Amina dapat mempunyai sifat basa karena mampu menyumbangkan sepasang electron bebasnya, sehingga semakin banyak senyawa amina yang disubstitusi oleh gugus alkil maka sifat kebasaan dari amina tersebut semakin kuat. Karena gugus yang melepaskan electron dapat menstabilkan muatan positif dari ion amonium. Sehingga jika direaksikan dengan asam, dan alkilasi yang terjadi secara berulang-ulang akan menghasilkan amina dengan produk samping suatu garam ammonium kuartener.
Pada aldehida atau keton terdapat sebuah gugus karbonil. Sehingga kepolaran dari gugus karbonil ini mengakibatkan titik didih dari aldehida dan keton terdapat diantara senyawa yang nonpolar atau senyawa yang memiliki ikatan hidrogen. Senyawa aldehida dan keton mempunyai kelarutan yang hamper sama antara larut dalam air dan dalam alkohol. Aldehida dan keton dapat melangsungkan reaksi adisi, seperti hydrogen asikatalitik, reaksi katalitik asam dengan nukleofil lemah, dan sebagainya. Reaktifitas senyawa karbonil akan bertambah jika substitusi dari karbon karbonil berkurang.
Cara Kerja
Method
Alat dan Bahan
Alat
Erlenmeyer
bekerglass
mechanical stirrer
magnetic stirrer
thermometer
Corong Buchner
Bahan
Urea
HCl 2N
Es
Aquadest
Cara Kerja
Dimasukkan sebanyak 10,2 mL benzaldehid kedalam Erlenmeyer yang didalamnya telah ada magnetic stirrer. Ditambahkan 3 g urea yang telah dilarutan dalam aquadest, dimasukkan kedalam campuran pertama tadi. Ditambahkan larutan HCl 4-5 tetes kedalam campuran larutan diatas, atau sampai mencapai pH 3. Diaduk campuran larutan tersebut selama 30 menit, dan suhu dalam Erlenmeyer dijaga antara 15 , sampai terbentuk endapan putih (seperti krim). Diaduk campuran pada suhu kamar, tanpa dijaga suhunya selama kurang lebih 30 menit. Disaring endapan yang terbentuk menggunakan corong Buchner, jika masih ada yang menempel pada erlenmeyer diencerkan dengan aquadest dingin. Ditimbang berat basah, dikeringkan, kemudian ditimbang berat kering dan di hitung titik leburnya. Dihitung hasil rendemen (dalam %).
, sampai terbentuk endapan putih (seperti krim). Diaduk campuran pada suhu kamar, tanpa dijaga suhunya selama kurang lebih 30 menit. Disaring endapan yang terbentuk menggunakan corong Buchner, jika masih ada yang menempel pada erlenmeyer diencerkan dengan aquadest dingin. Ditimbang berat basah, dikeringkan, kemudian ditimbang berat kering dan di hitung titik leburnya. Dihitung hasil rendemen (dalam %).
Hasil dan Pembahasan
Result and Discussion
Hasil
No
|
Kelompok
|
Berat Kering
|
% Rendemen (b/b)
|
Titik Lebur
|
1
|
H.1
|
4,19 gram
|
35,33 %
|
110°-121° C
|
2
|
H.2
|
5,86 gram
|
49,66 %
|
128°-138° C
|
3
|
H.3
|
3,75 gram
|
23,30 %
|
110°-120° C
|
4
|
H.4
|
8,65 gram
|
73,31 %
|
112°-129° C
|
5
|
H.5
|
7,86 gram
|
66,61 %
|
88°-100° C
|
6
|
H.6
|
1,36 gram
|
11,50 %
|
100°-108° C
|
Rata-rata
|
5,28 gram
|
43,29 %
|
Pembahasan
Pembuatan 1,3-bis-Fenilmetilidinurea dilakukan dengan cara adisi-eliminasi dari benzaldehid dan urea. Dengan prinsip reaksi adisi-eliminasi suatu nukleofil menyerang gugus karbonil. Gugus karbonil tersebut berasal dari benzaldehid sedangkan urea berfungsi sebagai nukleofil dan dengan bantuan HCl 2N sebagai kalatis dan dapat mempercepat reaksi serta dapat mengadisi nukleofilik. Mekanisme pembuatan imina merupakan proses dua tahap. Tahap pertama yaitu adisi amina nukleofil pada karbon karbonil positif parsial.
Tahap kedua (eliminasi) yaitu pelepasan gugus OH sebagai molekul air dan pembentukan ikatan rangkap nitrogen untuk menghasilkan imina.
Pembuatannya adalah pertama menyiapkan semua bahan dimasukkan benzaldehid (10,2 mL) dan urea (3 g) dalam erlenmeyer ditutup dengan aluminium foil agar urea tidak menguap dengan udara. Sebelum dicampur dengan benzaldehid, maka urea dilarutkan dengan air. Karena pH larutan belum asam maka ditambahkan HCl 2N sebanyak 1 tetes diukur pH agar pH 4 dengan indikator pH agar reaksi berlangsung optimal. Didalam erlenmeyer diletakkan pengaduk magnetik kemudian distirer selama 30 menit dengan suhu dijaga 15°C. Apabila telah terbentuk endapan maka diaduk kembali dengan suhu ruang (36°-37°C) selama 30 menit. Disaring larutan dengan corong buchner, ditimbang dan dikeringkan terbentuk 1,3-bis-Fenilmetilidinurea yang berbentuk serbuk dengan warna putih dan bau khas menyengat.
Dan dari data yang kami ambil dari seluruh kelompok, didapat kelompok empat menunjukkan berat yang paling banyak yaitu 8,65 g dengan rendemen 73,31%. Serta hasil titik lebur yang menunjukkan titik 88°-138° C. Dan berat kering secara teoritis yaitu 11,8 gram sedangkan titik lebur teoritis belum diketahui.
Kesimpulan
Conclusion
Dari praktikum yang telah dilakukan didapatkan hasil produk yang berbentuk serbuk dengan warna putih dan bau khas menyengat dari reaksi adisi-eliminasi benzaldehid dengan urea. Berat kering rata-rata yang didapat yaitu 5,28 gram dengan rata-rata rendemen 43,29 % b/b yang lebih kecil dari berat kering teoritis yaitu 11,8 gram.
PERMASALAHAN
1. Alkaloid adalah senyawa yang mengandung nitrogen yang bersifat basa dari tumbuhan atau hewan , salah satu penghasil alkaloid yang berarti adalah katak beracun .Katak ini mensekresikan alkaloid beracun dari permukaan kulitnya . yang paling beracun dari sekresi ini adalah batrakotoksin , bagaimana proses terjadinya batrakotoksin dalam sekresi permukaan kulit katak sehingga bisa menghasilkan senyawa yang alkaloid yang sangat beracun sementarabiasanya alkaloid digunakan untuk bahan obat- obatan . bagaimana struktur amina dalam btrakotoksin tersebut ???
2. Bagaimana amina dapat mengalami delokalisasi elektron. dan kenapa hal tersebut dapat menyebabkan sifat kebasaan amina?
3. Pada pemutusan gugus triofluoro asetamida itukan digunakan refluks,apakah refluks disini berpengaruh terhadap peningkatan proses deproteksi atau bagaimana?? selanjutnya apakah masih ada proteksi gugus amina lain?

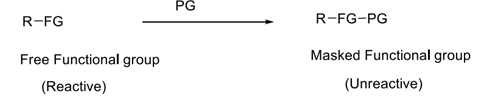
Saya akan menjawab permasalahan 3. refluks disana berfungsi agar selama reaksi berlangsung uap yang dihasilkan dari pemanasan kembali kedalam labu, dimana uap tersebut berupa metanol yang menjadi pelarut dalam reaksi tersbut sehingga dengan dilakukanya refluks maka proses deproteksi akan berjalan lebih baik dengan jumlah pelarut yang tidak berkurang. selanjutnya menjawab pertanyaan apakah ada gugus proteksi amina selain yang dijelaskan diatas untuk saat ini data dari gugs pelindung amina yang diketahui adalah seprti diatas, tapi tidak menutup kemungkinan akan ditemukan gugus pelindung lain.
BalasHapusSaya akan menjawab permasalahan yang kedua, 6qng mana suatu Amina memiliki pasangan elektron bebas, apabila amina primer misal Ar-NH2, amina primer ini mengikat satu gugus phenil, gugus phenil tersebutlah yang mengakibatkan amina mengalami delokalisasi elektron
BalasHapusPermasalahan 3reaksi refluks pada proses deproteksi akan berjalan lebih baik dengan jumlah pelarut yang tidak berkurang.
BalasHapusSaya akan mencoba menjawab permasalahan Anda yg ke-2:
BalasHapussuatu Amina memiliki pasangan elektron bebas, apabila amina primer misal Ar-NH2, amina primer ini mengikat satu gugus phenil, gugus phenil tersebutlah yang mengakibatkan amina mengalami delokalisasi elektron.
Saya akan menjawab permasalahan yang kedua, yang mana suatu Amina memiliki pasangan elektron bebas, apabila amina primer misal Ar-NH2, amina primer ini mengikat satu gugus phenil, gugus phenil tersebutlah yang mengakibatkan amina mengalami delokalisasi elektron
BalasHapusSaya akan mencoba menjawab permasalahan Anda yg ke-2:
BalasHapussuatu Amina memiliki pasangan elektron bebas, apabila amina primer misal Ar-NH2, amina primer ini mengikat satu gugus phenil, gugus phenil tersebutlah yang mengakibatkan amina mengalami delokalisasi elektron.
refluks disana berfungsi agar selama reaksi berlangsung uap yang dihasilkan dari pemanasan kembali kedalam labu, dimana uap tersebut berupa metanol yang menjadi pelarut dalam reaksi tersbut sehingga dengan dilakukanya refluks maka proses deproteksi akan berjalan lebih baik dengan jumlah pelarut yang tidak berkurang. selanjutnya menjawab pertanyaan apakah ada gugus proteksi amina selain yang dijelaskan diatas untuk saat ini data dari gugs pelindung amina yang diketahui adalah seprti diatas,
BalasHapusSaya akan menjawab permasalahan yang kedua, yang mana suatu Amina memiliki pasangan elektron bebas, apabila amina primer misal Ar-NH2, amina primer ini mengikat satu gugus phenil, gugus phenil tersebutlah yang mengakibatkan amina mengalami delokalisasi elektron
BalasHapusSaya akan menjawab permasalahan yang kedua, 6qng mana suatu Amina memiliki pasangan elektron bebas, apabila amina primer misal Ar-NH2, amina primer ini mengikat satu gugus phenil, gugus phenil tersebutlah yang mengakibatkan amina mengalami delokalisasi elektron
BalasHapusSaya akan mencoba menjawab permasalahan Anda yg ke-2:
BalasHapussuatu Amina memiliki pasangan elektron bebas, apabila amina primer misal Ar-NH2, amina primer ini mengikat satu gugus phenil, gugus phenil tersebutlah yang mengakibatkan amina mengalami delokalisasi elektron.
Saya akan menjawab permasalahan 3. refluks disana berfungsi agar selama reaksi berlangsung uap yang dihasilkan dari pemanasan kembali kedalam labu, dimana uap tersebut berupa metanol yang menjadi pelarut dalam reaksi tersbut sehingga dengan dilakukanya refluks maka proses deproteksi akan berjalan lebih baik dengan jumlah pelarut yang tidak berkurang
BalasHapusNo 3 refluks disana berfungsi agar selama reaksi berlangsung uap yang dihasilkan dari pemanasan kembali kedalam labu, dimana uap tersebut berupa metanol yang menjadi pelarut dalam reaksi tersbut sehingga dengan dilakukanya refluks maka proses deproteksi akan berjalan lebih baik dengan jumlah pelarut yang tidak berkurang.
BalasHapusjawaban permasalahan no 2 Karena itu mempunyai ikatan NH, amina tersier dalam bentuk cairan murni tidak dapat membentuk ikatan hidrogen. Titik didih amina tersier lebih rendah dari pada amina primer atau sekunder yang bobot melekulnya sepadan, dan titik didihnya lebih dekat ke titik didih alkana yang bobot molekulnya bersamaan. Dan amina yang berbobot molekul rendah larut dalam air karena membentuk ikatan hidrogen dengan air. Amina tersier maupun amina sekunder dan primer dapat membentuk ikatan hidrogen karena memiliki pasangan elektron menyendiri yang dapat digunakan untuk membentukikatan hidrogen dengan air.
BalasHapusDan berikut merupakan beberapa sifat fisis amina